
La última vez que la tabla periódica incorporó nuevos elementos fue hace una década.
En ese entonces, los elementos 113, 115, 117 y 118 se ganaron su lugar en la famosa cuadrícula.
Además, la Unión Internacional de Química Pura y Aplicada (IUPAC), el organismo internacional que supervisa este instrumento, hizo en aquel 2016 algo que solo se había atrevido a hacer una vez anteriormente: bautizó uno de los elementos con el nombre de un físico vivo.
Yuri Oganessian dirigió el grupo de investigación rusoestadounidense que en 2002 descubrió el elemento 118, al que llamaron oganesón.
No obstante, se tardó años en confirmar el hallazgo, porque el elemento es tan radiactivo que solo se han creado unos pocos átomos.
Uno podría preguntarse por qué no se han añadido nuevos elementos en estos 10 años que han transcurrido y si alguna vez podrá decirse que la tabla periódica está completa.
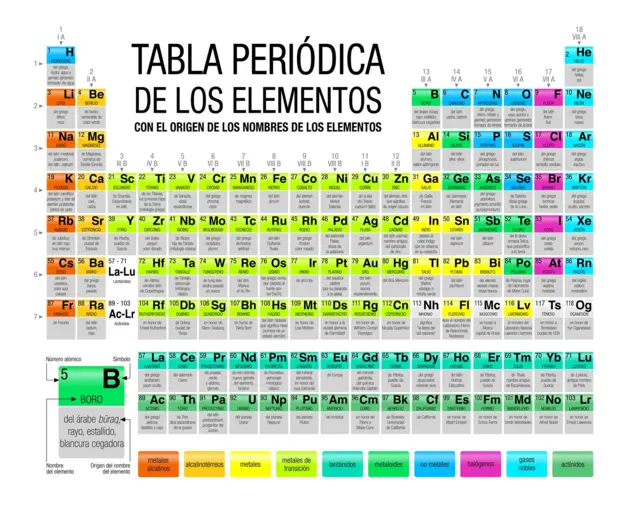
¿Qué es la tabla periódica?
La tabla periódica es, en esencia, un mapa de elementos químicos con muchos cuadrados rellenos con sus abreviaturas, también conocidas como símbolos químicos. Y se ha ido actualizando a lo largo de los años.
Un elemento es una sustancia pura compuesta por un solo tipo de átomo.
Final de Más leídas
Los átomos son los componentes básicos de la materia y tienen un núcleo, que generalmente contiene protones con carga positiva y neutrones sin carga, rodeado de electrones con carga negativa.
Los elementos de la tabla periódica, en conjunto, conforman todo lo que conocemos en el universo, incluidos nosotros mismos.
A principios del siglo XIX ya se habían descubierto muchos elementos, pero no estaban organizados de forma sistemática. Varios pioneros de la tabla periódica intentaron cambiar esta situación.
Uno de ellos fue el químico británico John Newlands.
Ordenó los elementos por peso atómico (una medida de la masa del átomo) y observó que cada octavo elemento tenía propiedades similares. Por ejemplo, el litio, el sodio y el potasio están separados por ocho posiciones y muestran reacciones similares con el agua.
A esto lo denominó ley de las octavas.

Fin de Podcast
El químico ruso Dmitri Mendeléyev (Mendeleev en su idioma original), ampliamente conocido como el padre de la tabla periódica, tomó la idea de las propiedades recurrentes y formuló lo que se conoce como la ley periódica.
En 1869 elaboró un esquema para la tabla periódica moderna, con los elementos ordenados por peso atómico.
A diferencia de la versión de Newlands, dejó espacios para los elementos que faltaban y su trabajo cobró relevancia cuando estos elementos fueron descubiertos posteriormente.
Hoy los elementos de la tabla periódica se definen y organizan según su número atómico, es decir, el número de protones del núcleo.
El hidrógeno tiene un protón, por ejemplo, mientras que el oganesón tiene 118.
Los elementos de una misma columna tienen propiedades químicas similares, como la forma en que reaccionan con otras sustancias.
A menudo también siguen un patrón en sus propiedades físicas, como el punto de fusión, lo que ayuda a los científicos a predecir su comportamiento.
Los ingenieros, por ejemplo, pueden utilizar la tabla periódica para seleccionar materiales al diseñar puentes y aviones.

Si un científico cree haber identificado un nuevo elemento, la IUPAC verifica si existe y se le concede un lugar en la tabla, un proceso que puede tardar años.
Se cree que hemos encontrado todos los elementos que se dan de forma natural en la Tierra, los cuales constituyen la mayor parte de la tabla.
Los elementos más pesados deben crearse artificialmente en el laboratorio combinando dos más ligeros.
Los científicos han podido añadir cada vez más elementos superpesados gracias a los avances tecnológicos. Pero, aunque en teoría los humanos podrían seguir intentando crear otros nuevos, cada vez resulta más difícil.
Creación de nuevos elementos
Para fusionar elementos más ligeros y crear otros nuevos cada vez más grandes, "tenemos que alcanzar condiciones de energía cada vez más elevadas, construyendo ciclotrones o aceleradores cada vez más grandes", explica Phil Blower, director del Departamento de Química y Biología de Imagen del King's College de Londres.
"A medida que los elementos se hacen cada vez más grandes y pesados, se vuelven cada vez menos estables debido a los protones del núcleo", afirma Blower.
La proporción de protones y neutrones en un núcleo determina si será estable o inestable.
Los protones, con carga positiva, se repelen entre sí de forma natural, pero la presencia de neutrones puede mantenerlos unidos.

"Lo que se hace al crear elementos cada vez más pesados es añadir más protones al núcleo, y para evitar que se desintegre, se necesita un número cada vez mayor de neutrones", explica Cinzia Imberti, líder del grupo de Imaging Metallomics del King's College de Londres.
Un elemento puede existir con diferentes números de neutrones. Estas variaciones se denominan isótopos.
Los isótopos inestables son radiactivos: se desintegran al emitir radiación.
"Todos los elementos más pesados que el plomo (elemento 82) son radiactivos, son intrínsecamente inestables y se descomponen", explica Jonathan Rourke, químico de la Universidad de Cardiff y profesor honorario de la Universidad de Warwick en Reino Unido.
"Si fuéramos capaces de crear un solo átomo de uno de esos elementos, no duraría mucho tiempo", explica.
Eso es especialmente cierto a partir del elemento 100 (fermio) dice Imberti.
"Si creas unos pocos átomos, puedes averiguar algo sobre ellos, quizá sus propiedades físicas. Pero no tienen ningún uso práctico", explica.
No obstante, la búsqueda de los próximos elementos (los cuales llevarían a la tabla periódica a una nueva fila) sigue en marcha.
Muchos intentos por encontrar los números 119 y 120 han fracasado hasta ahora, pero varios grupos de investigación siguen intentándolo.
Los científicos afirman que explorar los elementos en los extremos podría proporcionarnos nuevos conocimientos sobre cómo funcionan los átomos, los límites de los núcleos atómicos y la oportunidad de poner a prueba teorías sobre la física nuclear.
Imberti explica: "Hay que pensar no solo en si podemos crearlo, sino en si puede durar lo suficiente como para que podamos descubrirlo de forma significativa, aprender un poco sobre él... antes de que desaparezca".








0 Comentarios